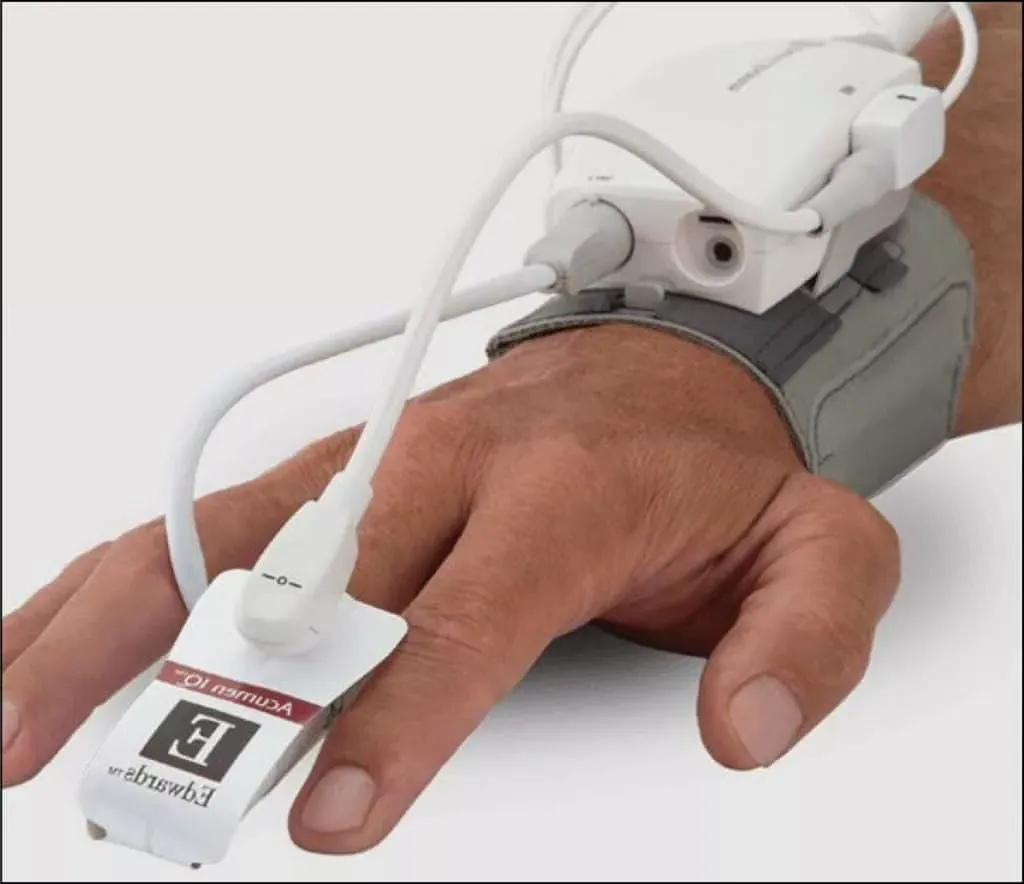
体外诊断设备(IVDD)简介
体外诊断设备(IVDD)在现代医疗保健中起着至关重要的作用,有助于早期发现, 诊断。, 以及疾病监测. 这些设备用于分析血液等样本, 尿液, 和组织提供有价值的信息,帮助医疗保健专业人员做出准确的医疗决定. 随着技术的进步, 这些设备的相关规定也是如此, 是什么将我们带到了体外诊断法规(IVDR)及其在确保IVDD安全性和有效性方面的重要性.
什么是IVDR,为什么它很重要?
体外诊断法规(IVDR)是欧盟(EU)为确保安全性而建立的监管框架, 表演。, 以及体外诊断设备的可靠性. 它取代了以前的体外诊断指令(IVDD),并对IVDD行业的制造商和其他利益相关者提出了更严格的要求.
IVDR的重要性在于其目的是通过提高质量来加强患者安全和公众健康, 安全, 以及体外诊断设备的性能. 遵从IVDR可确保这些设备经过彻底的评估, 符合特定标准, 并接受上市后监督,以发现任何潜在的风险或问题.
IVDR的关键法规和要求
IVDR引入了制造商和其他利益相关者必须遵守的几项关键法规和要求. 其中包括风险分类, 技术文档, 业绩评估, 上市后业绩跟踪和监督, 设备标识, 和唯一设备标识(UDI), 以及质量管理体系的要求.
了解IVD设备的风险分类
IVDR合规性的一个基本方面是根据其相关风险对体外诊断设备进行分类. IVDR将设备分为四类:A, B, C, 和D, D类设备的风险最高. 制造商必须为其设备确定适当的风险等级, 由于每个类别有不同的合格评定要求.
IVDR合规性的技术文档
制造商必须准备技术文件,证明其体外诊断设备符合IVDR法规. 该文档应包括有关器械设计的信息, 制造业, 表演。, 以及安全特性. 它作为器械经过适当测试和评估以确保其符合IVDR要求的证据.
绩效评估和绩效研究
IVDR强调进行性能评估和性能研究的重要性,以评估体外诊断设备的分析和临床性能. 这些评估和研究为该设备的准确性提供了证据, 可靠性, 以及临床用途. 制造商必须根据特定的标准进行这些评估,并记录结果,以证明符合IVDR.
上市后业绩跟踪和监督
上市后监督是IVDR合规性的一个关键方面. 它包括在体外诊断设备投放市场后对其性能和安全性进行监测. 制造商和其他利益相关者需要建立一个系统的过程来收集和分析设备性能的数据, 包括任何不良事件或事件. 这些数据用于识别任何潜在风险或问题,并采取适当的纠正措施以确保患者安全.
设备标签和唯一设备标识(UDI)
正确的设备标签和唯一设备标识(UDI)对于IVDR合规性至关重要. 制造商必须在其设备上提供清晰准确的标签, 包括预期用途等信息, 使用说明, 还有任何警告或预防措施. 另外, 每个设备必须有一个唯一的标识号(UDI),以便在其整个生命周期中易于跟踪和识别.
符合IVDR质量管理体系要求
确保始终遵守IVDR, 制造商必须建立和维持健全的质量管理体系(QMS). 该系统应涵盖设备生命周期的所有方面, 从设计和开发到制造, 分布, 以及上市后活动. 质量管理体系作为一个框架,确保所有流程和程序到位,以满足IVDR要求,并保持设备的安全性和有效性.
IVD设备的示例及其对IVDR的遵从性
为了更好地理解IVDR合规性的实际应用, 让我们来探讨一些体外诊断设备的例子,以及它们是如何遵守规定的. 这些例子包括血糖监测器等设备, 怀孕测试, 基因检测试剂盒, 和艾滋病诊断设备. 这些设备都属于特定的风险类别,需要遵守IVDR法规以确保其安全性和有效性.
IVDR合规性cq9电子游戏平台网址和资源
遵守IVDR可能是一个复杂的过程, 要求制造商和其他利益相关者通过各种法规和要求进行导航. 幸运的是, 有专门的IVDR合规cq9电子游戏平台网址和资源可以帮助您完成此过程. 这些cq9电子游戏平台网址提供指导, 培训, 并支持确保制造商理解并履行必要的IVDR义务. 另外, 监管机构和行业协会提供宝贵的资源和最新信息,帮助利益相关者了解情况并遵守IVDR.
结论
体外诊断法规(IVDR)合规性是确保安全的关键, 表演。, 以及体外诊断设备的可靠性. IVDR引入的法规和要求旨在通过提高质量来加强患者安全和公众健康, 安全, 以及这些设备的有效性. 通过了解关键规则, 比如风险分类, 技术文档, 业绩评估, 以及上市后监督, 制造商可以成功地驾驭合规流程. 利用IVDR合规性cq9电子游戏平台网址和资源进一步支持利益相关者履行其义务,并促进体外诊断的发展,以获得更好的医疗保健结果.
有关IVDR依从性及其对体外诊断设备的影响的更多信息,请 今天就cq9电子游戏平台网址的专家.